Résumé : L'amélioration des plantes entre dans une ère nouvelle, où les outils biotechnologiques les plus avancés s'associent aux approches conventionnelles pour accélérer le progrès génétique. Les techniques d'édition génomique comme CRISPR/Cas9, désormais déployées sur une vaste gamme de cultures, permettent des modifications précises du génome sans introduction d'ADN étranger, avec des applications allant de la résistance aux stress biotiques et abiotiques à l'amélioration de la qualité nutritionnelle . La sélection génomique (Genomic Selection), qui utilise des marqueurs couvrant l'ensemble du génome pour prédire la valeur génétique des individus, révolutionne les programmes de sélection en réduisant les cycles de sélection de plusieurs années . L'intégration de l'intelligence artificielle et du phénotypage haut débit (drones, capteurs, imagerie) permet d'exploiter des volumes de données sans précédent pour guider les décisions de sélection . Par ailleurs, la redécouverte des ressources génétiques conservées dans les banques de gènes (comme celles du CGIAR, qui abritent plus de 700 000 échantillons) offre un réservoir de diversité précieux pour l'adaptation au changement climatique . Les premiers produits issus de ces nouvelles approches commencent à arriver sur le marché, dans un contexte réglementaire en pleine évolution, notamment en Europe avec la proposition de règlement sur les plantes issues de nouvelles techniques génomiques (NGT) . Cet article explore ces différentes technologies, leurs applications concrètes, les défis scientifiques et réglementaires, et les perspectives pour une agriculture durable et résiliente.
1. L'édition génomique : une révolution dans la précision
1.1 CRISPR/Cas9 et ses dérivés : des ciseaux moléculaires de précision
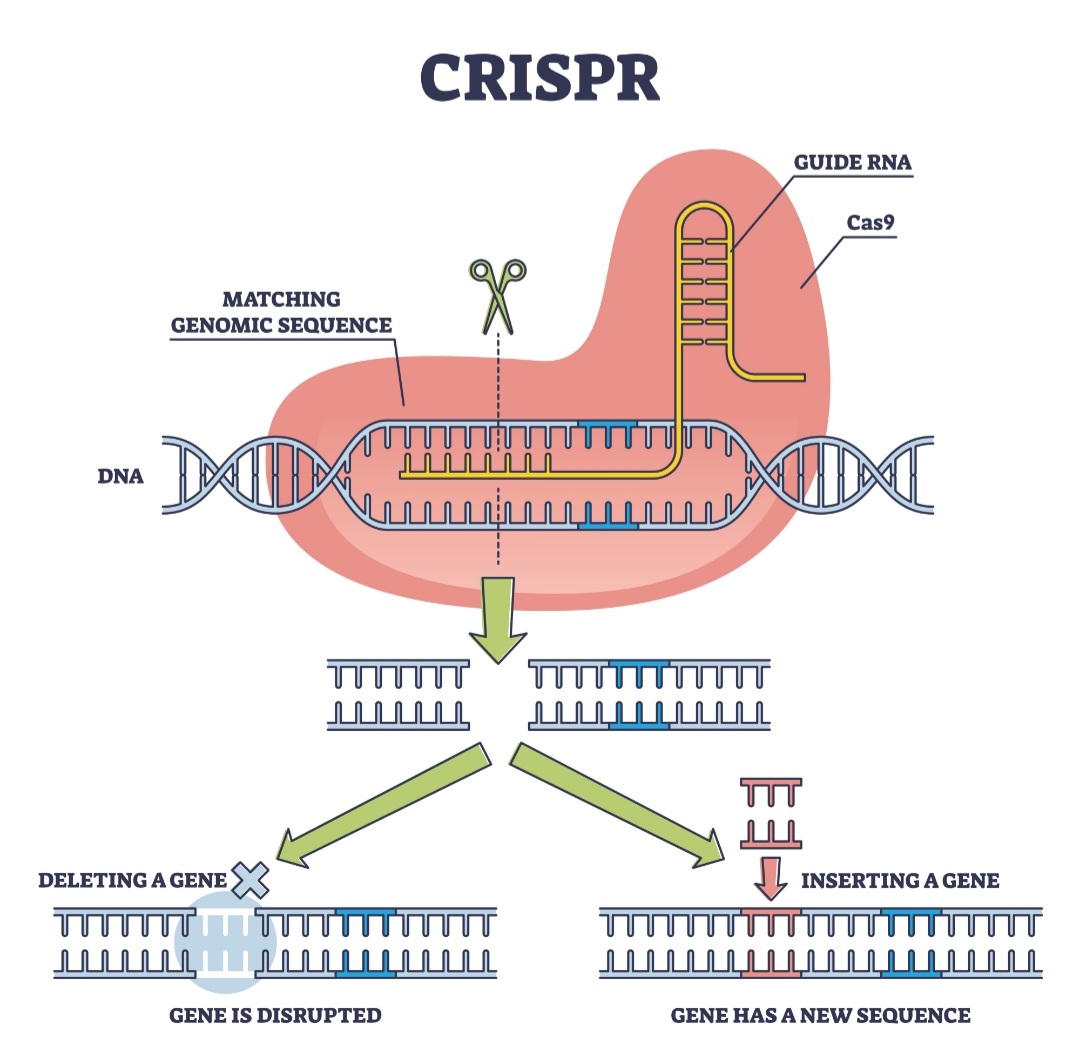
CRISPR (Clustered Regularly Interspaced Short Palindromic Repeats) est une technologie d'édition du génome qui permet de modifier de manière ciblée l'ADN des organismes vivants . Découverte à partir d'un système immunitaire bactérien, elle a été adaptée comme outil de modification génétique pour son efficacité, sa simplicité et sa précision .
Le principe : une enzyme (Cas9) agit comme des "ciseaux moléculaires" capables de couper l'ADN à un endroit précis, guidée par un ARN (guide ARN) conçu pour reconnaître une séquence spécifique. La cellule répare ensuite la coupure, ce qui permet soit d'inactiver un gène (knock-out), soit d'introduire une nouvelle séquence (knock-in) .
Les avantages par rapport aux OGM transgéniques classiques sont majeurs :
· Précision : modification à un endroit exact du génome
· Absence d'ADN étranger : dans certaines applications, le produit final ne contient aucune séquence exogène
· Multiplexage : possibilité de cibler plusieurs gènes simultanément
· Rapidité : cycles de développement plus courts qu'en sélection conventionnelle
1.2 Applications concrètes de l'édition génomique en agriculture
Résistance aux maladies :
Des chercheurs ont utilisé CRISPR pour créer des variétés de riz résistantes à la pyriculariose, l'une des maladies les plus dévastatrices, en ciblant des gènes de sensibilité du riz . Aux États-Unis, des variétés de blé résistantes à l'oïdium ont été développées par édition du gène de sensibilité MLO .
Tolérance aux stress abiotiques :
Au Brésil, une équipe a développé des plants de canne à sucre tolérants à la sécheresse en surexprimant le gène ScTpx2, maintenant des taux de photosynthèse 12 à 23 % plus élevés que les plants sauvages sous stress hydrique . En Chine, des chercheurs ont amélioré la tolérance à la sécheresse du millet en inactivant le gène SiZAT12, sans pénalité de rendement .
Amélioration de la qualité nutritionnelle :
Le Japon a commercialisé en 2021 une tomate CRISPR avec une teneur élevée en GABA (acide gamma-aminobutyrique), un acide aminé aux propriétés relaxantes . Aux États-Unis, des variétés de soja à l'huile améliorée (acides gras oméga-3) sont en développement .
Caractéristiques agronomiques :
Des variétés de pomme de terre avec une teneur réduite en asparagine (précurseur de l'acrylamide lors de la friture) ont été développées par édition génomique, permettant de réduire la formation de composés potentiellement cancérigènes .
1.3 Le contexte réglementaire : l'exemple européen
En Europe, le statut des plantes issues de l'édition génomique est actuellement en pleine évolution. L'arrêt de la Cour de justice de l'Union européenne de 2018 a statué que les plantes obtenues par mutagenèse dirigée (dont CRISPR) devaient être considérées comme des OGM et soumises à la réglementation correspondante .
Cependant, une proposition de règlement de la Commission européenne (2023) propose de créer une nouvelle catégorie pour les "plantes issues de nouvelles techniques génomiques (NGT)" de catégorie 1 (mutations ponctuelles ou insertions de gènes de la même espèce), avec un régime allégé par rapport aux OGM transgéniques . Cette proposition est actuellement en discussion au Parlement européen et au Conseil.
Dans d'autres régions du monde, le cadre est plus favorable :
· États-Unis : les plantes CRISPR ne sont pas réglementées si elles ne contiennent pas d'ADN étranger (approche "produit" basée sur les caractéristiques)
· Canada : approche similaire, évaluation au cas par cas
· Japon : régulation allégée, premières commercialisations
· Royaume-Uni : sorti de l'UE, le pays a adopté une législation plus permissive via le Genetic Technology Act
2. La sélection génomique : accélérer le progrès génétique
2.1 Principes et avantages
La sélection génomique (Genomic Selection) est une méthode qui utilise des marqueurs génétiques répartis sur l'ensemble du génome pour prédire la valeur génétique d'un individu . Contrairement à la sélection assistée par marqueurs (MAS) qui cible quelques gènes majeurs, la sélection génomique prend en compte l'effet de l'ensemble des gènes (y compris ceux à faible effet).
Le processus :
1. Population de référence : un panel d'individus est génotypé et phénotypé pour les caractères d'intérêt
2. Modèle prédictif : un modèle statistique (ex : GBLUP, Bayesian) est entraîné pour estimer l'effet de chaque marqueur
3. Prédiction : les individus à sélectionner sont génotypés (mais pas phénotypés) et leur valeur génétique est prédite par le modèle
4. Sélection : choix des meilleurs individus sur la base des prédictions
Avantages :
· Accélération du cycle de sélection : pas besoin d'attendre le phénotypage pour sélectionner, passage de 10-15 ans à 5-8 ans pour une nouvelle variété
· Efficacité pour les caractères complexes (rendement, tolérance aux stress) contrôlés par de nombreux gènes
· Précision accrue par rapport aux méthodes conventionnelles
2.2 La sélection génomique environnementale (enviromics)
Une avancée récente est l'intégration des données environnementales dans les modèles de prédiction. La sélection génomique environnementale (ou enviromics) intègre des variables climatiques, pédologiques et de conduite culturale pour prédire la performance des génotypes dans différents environnements .
Des modèles comme GS+E (Genomic Selection + Environment) permettent :
· D'identifier les génotypes les plus adaptés à un territoire spécifique
· De prédire la stabilité des performances dans différents contextes climatiques
· D'optimiser le déploiement variétal (recommendation variétale de précision)
2.3 L'intégration avec l'IA et le phénotypage haut débit
Le phénotypage est traditionnellement le goulot d'étranglement de la sélection génomique. Les nouvelles technologies de phénotypage haut débit (High-Throughput Phenotyping) lèvent ce verrou :
Technologie Application
Drones équipés de capteurs multispectraux Mesure de la biomasse, indices de végétation, stress hydrique
Capteurs LiDAR Hauteur des plantes, architecture du couvert
Caméras thermiques Température de surface, stress hydrique
Spectromètres proche infrarouge (NIR) Composition chimique (protéines, amidon)
Imagerie hyperspectrale Détection précoce de maladies, stress nutritionnel
Ces technologies génèrent des millions de données par parcelle, qui sont ensuite analysées par des algorithmes d'apprentissage automatique (machine learning) pour extraire les informations pertinentes sur les caractères d'intérêt. Des modèles de deep learning (réseaux de neurones convolutifs) sont utilisés pour analyser les images et quantifier des caractères comme le nombre d'épis par m² ou la sévérité de maladie .
3. Les ressources génétiques : un réservoir de diversité pour l'adaptation
3.1 L'importance des banques de gènes
Les banques de gènes (ou cryobanques) conservent des échantillons de semences, de tissus ou de pollen représentant la diversité génétique des espèces cultivées et de leurs parents sauvages. Le système du CGIAR (Groupe consultatif pour la recherche agricole internationale) gère plus de 700 000 échantillons de céréales, légumineuses, racines et tubercules dans ses 11 banques de gènes .
Ces collections sont essentielles car :
· Elles contiennent des variétés locales et des parents sauvages adaptés à des conditions extrêmes (sécheresse, salinité, chaleur)
· Elles permettent de retrouver des gènes perdus dans les variétés modernes lors de la sélection
· Elles sont une ressource pour l'adaptation au changement climatique
3.2 La redécouverte des variétés locales
Dans de nombreux pays, les variétés locales (landraces) sont redécouvertes pour leur potentiel d'adaptation. Une étude espagnole sur le maïs a évalué la collection nationale pour la tolérance à la sécheresse, identifiant des variétés comme Villanueva del Arzobispo (popcorn) et Cacheira, Cima, Acibeiro (maïs grain) qui combinent stabilité et rendement élevés sous stress hydrique . Ces variétés traditionnelles présentent une diversité génétique précieuse, souvent perdue dans les cultivars modernes.
3.3 L'exploration des espèces sauvages apparentées
Les parents sauvages des espèces cultivées (Crop Wild Relatives) sont une source de gènes de résistance et de tolérance souvent inexploitée. Des programmes comme le Crop Wild Relatives Project du CGIAR ont collecté et caractérisé des centaines d'espèces sauvages apparentées au blé, au riz, au haricot, à la pomme de terre et à la banane .
Des gènes de résistance aux maladies (rouille du blé, mildiou de la pomme de terre) ont été transférés des parents sauvages vers les variétés cultivées via des croisements assistés par marqueurs. La tolérance à la sécheresse et à la chaleur chez le sorgho et le millet provient également de ces ressources .
4. Les approches omiques : comprendre le vivant dans sa globalité
4.1 Génomique, transcriptomique, protéomique, métabolomique
Les approches "omiques" étudient les différents niveaux d'expression de l'information génétique :
Domaine Objet d'étude Applications en amélioration
Génomique Ensemble des gènes Cartographie des QTL, séquençage d'espèces, détection de variants
Transcriptomique ARN messagers (expression des gènes) Identification de gènes induits par un stress, marqueurs d'expression
Protéomique Ensemble des protéines Fonction des gènes, interactions protéine-protéine
Métabolomique Ensemble des métabolites Qualité nutritionnelle, biomarqueurs de stress
L'intégration de ces données (multi-omiques) permet une compréhension systémique du fonctionnement de la plante, indispensable pour identifier des cibles pour l'édition génomique et développer des modèles prédictifs performants .
4.2 La découverte de gènes d'origine microbienne
Une approche novatrice consiste à explorer le génome des micro-organismes associés aux plantes (microbiote) pour y trouver des gènes utiles. Le concept de CRISPR-enabled Horizontal Gene Transfer (CRISPR-HGT) propose de transférer des gènes d'origine bactérienne ou fongique vers les plantes cultivées, en utilisant CRISPR pour l'intégration précise .
Pourquoi les microbes ? Parce qu'ils sont confrontés depuis des millions d'années aux mêmes stress (sécheresse, chaleur, salinité) et ont développé des gènes de résistance éprouvés. Une étude marquante a révélé que le blé et ses proches parents possèdent des gènes de protéines de choc froid (CSP) d'origine bactérienne, contribuant à une meilleure tolérance à la sécheresse .
5. La convergence des technologies : vers une amélioration accélérée
5.1 Le modèle de la "speed breeding"
La "speed breeding" (sélection accélérée) combine des conditions de culture contrôlées (photopériode longue, température optimale) pour réduire la durée des cycles de sélection. Chez le blé, on peut passer de 2-3 cycles par an en conditions normales à 6-7 cycles par an en speed breeding .
Associée à la sélection génomique et à l'édition génomique, la speed breeding permet de réduire le temps de développement d'une nouvelle variété de 10-15 ans à 3-5 ans.
5.2 L'intégration de l'IA dans les pipelines de sélection
L'intelligence artificielle (IA) est en train de transformer l'ensemble du processus de sélection :
· Découverte de gènes : des modèles d'apprentissage profond analysent les données multi-omiques pour prédire quels gènes sont impliqués dans des caractères d'intérêt
· Prédiction de la valeur génétique : des algorithmes de machine learning (Random Forest, Gradient Boosting) surpassent parfois les modèles statistiques classiques pour la prédiction génomique
· Analyse d'images : des réseaux de neurones convolutifs (CNN) analysent les images de plantes pour quantifier des caractères complexes (nombre de grains par épi, symptômes de maladie)
· Optimisation des croisements : des algorithmes d'optimisation suggèrent les croisements les plus prometteurs pour générer de nouvelles combinaisons génétiques
5.3 Les premiers succès commerciaux
Plusieurs produits issus de ces nouvelles approches sont déjà sur le marché ou en phase avancée de développement :
Produit Caractéristique Technologie Statut
Tomate GABA Teneur élevée en GABA CRISPR Commercialisée au Japon (2021)
Soja à huile améliorée Acides gras oméga-3 CRISPR En développement (US)
Pomme de terre "Innate" Réduction acrylamide CRISPR Autorisation US (2015)
Blé résistant oïdium Inactivation MLO CRISPR Essais terrain (US, Europe)
Maïs tolérant sécheresse Édition gènes mélatonine CRISPR Recherche avancée (Chine)
6. Défis et perspectives
6.1 Défis scientifiques et techniques
Défi Description Solutions
Efficacité de transformation Toutes les variétés ne se prêtent pas à l'édition génomique Développement de protocules variétaux, approches de transformation in planta
Effets hors cible (off-target) Risque de coupures à des endroits non désirés Amélioration des enzymes Cas (Cas9 haute fidélité), validation par séquençage
Caractères complexes La résistance à la sécheresse implique de nombreux gènes Approches multiplexées (cibler plusieurs gènes)
Transfert vers les filières Valorisation des variétés améliorées dans les chaînes de production Collaboration sélectionneurs-filières dès la phase de recherche
6.2 Défis réglementaires et sociétaux
Le blocage européen : L'arrêt de la CJUE de 2018 a eu un effet dissuasif sur la recherche et le développement en Europe. De nombreuses équipes ont délocalisé leurs travaux ou se sont tournées vers d'autres marchés. La proposition de règlement NGT est donc attendue avec impatience par la communauté scientifique et les sélectionneurs .
L'acceptabilité sociale : La distinction subtile entre édition génomique et OGM transgénique n'est pas toujours comprise du grand public. La communication sur les bénéfices (réduction des pesticides, adaptation au changement climatique) est essentielle, de même que la transparence sur les méthodes utilisées.
La propriété intellectuelle : Les brevets sur CRISPR-Cas9 (notamment ceux du Broad Institute et de l'UC Berkeley) ont été très disputés. Des mécanismes de licences ouvertes (comme ceux mis en place pour les technologies du blé) sont nécessaires pour éviter un verrouillage de l'innovation.
6.3 Perspectives d'avenir
L'intégration des ressources génétiques : La combinaison de l'exploration des banques de gènes, de la sélection génomique et de l'édition génomique permettra d'exploiter la diversité naturelle de manière inédite. Le projet "Seeds for the Future" du CGIAR vise à évaluer l'ensemble de la collection de blé (plus de 100 000 échantillons) pour identifier des sources de tolérance aux stress .
L'adaptation aux stress combinés : Le changement climatique expose les cultures à des combinaisons de stress (chaleur + sécheresse + salinité). L'édition génomique multiplexée permettra de créer des variétés résistantes à ces stress multiples .
La transition vers une agriculture régénérative : Les nouvelles variétés ne sont pas une fin en soi. Leur déploiement s'inscrit dans des systèmes de culture plus durables (non-labour, couverts végétaux, agroforesterie), créant des synergies bénéfiques pour la santé des sols et la biodiversité.
7. Recommandations pour les acteurs du secteur
7.1 Pour les pouvoirs publics
1. Clarifier le cadre réglementaire : adopter une proposition de règlement NGT qui permette de distinguer les plantes issues d'édition génomique sans ADN étranger des OGM transgéniques, afin de ne pas freiner l'innovation en Europe .
2. Soutenir la recherche publique : financer les programmes de recherche sur la sélection génomique, l'édition génomique et le phénotypage haut débit, ainsi que la conservation et la caractérisation des ressources génétiques.
3. Faciliter l'accès aux banques de gènes et encourager la collaboration internationale.
4. Soutenir la formation des sélectionneurs, des conseillers et des agriculteurs aux nouvelles technologies.
7.2 Pour les sélectionneurs et les entreprises
1. Investir dans les plateformes de phénotypage haut débit (drones, capteurs, analyse d'images) pour accélérer les cycles de sélection .
2. Développer des partenariats avec les laboratoires de recherche académique pour accéder aux technologies de pointe.
3. Adopter une approche intégrée combinant sélection conventionnelle, sélection génomique et édition génomique, sans opposer ces approches.
4. Anticiper les évolutions réglementaires en Europe pour être prêt le moment venu.
7.3 Pour les agriculteurs
1. S'informer sur les nouvelles variétés et leurs bénéfices (tolérance aux stress, réduction des intrants, qualité).
2. Participer aux essais variétaux pour évaluer les performances dans ses propres conditions.
3. S'engager dans des démarches de sélection participative pour orienter les programmes vers des besoins concrets.
8. Conseils pour les jeunes entrepreneurs
8.1 Opportunités identifiées
Domaine Opportunités
Services de phénotypage Prestations de phénotypage par drones, capteurs, analyse d'images pour les sélectionneurs et les instituts de recherche
Bio-informatique et IA Développement d'algorithmes pour l'analyse des données multi-omiques, la prédiction génomique, la détection de variants
Conseil réglementaire Accompagnement des entreprises pour les dossiers d'homologation, veille réglementaire, stratégies de mise sur le marché
Valorisation des ressources génétiques Exploration des banques de gènes pour identifier des sources de tolérance aux stress, développement de variétés adaptées aux marchés de niche
Formation Organisation de formations pour les sélectionneurs, les conseillers et les agriculteurs aux nouvelles technologies
Développement variétal pour niches Création de variétés adaptées à des marchés spécifiques (cultures locales, agriculture biologique, production sous serre)
8.2 Facteurs clés de succès
1. Maîtriser la double compétence biologie et numérique
Les nouvelles technologies d'amélioration des plantes se situent à l'intersection de la génétique, de la biologie moléculaire, de l'informatique et de la statistique. Une équipe pluridisciplinaire est indispensable.
2. S'appuyer sur les ressources publiques
Les banques de gènes, les collections de variétés locales, les données de séquençage publiques sont des ressources précieuses pour l'innovation. Les utiliser intelligemment permet de réduire les coûts de R&D.
3. Cibler des marchés spécifiques
Les grandes cultures (blé, maïs, soja) sont dominées par les multinationales. Des cultures de niche (légumineuses, plantes médicinales, espèces sous-utilisées) offrent des opportunités pour des startups agiles.
4. Anticiper les évolutions réglementaires
Le cadre réglementaire européen est en pleine mutation. Une veille active et une anticipation sont nécessaires pour positionner ses produits.
5. Communiquer sur les bénéfices
La transparence sur les méthodes utilisées et la communication sur les bénéfices (réduction des pesticides, adaptation au climat) sont essentielles pour l'acceptabilité.
Conclusion
La biotechnologie et l'amélioration avancée des plantes connaissent une révolution sans précédent. La convergence de l'édition génomique, de la sélection génomique, du phénotypage haut débit et de l'intelligence artificielle permet d'accélérer le progrès génétique comme jamais auparavant.
Les résultats sont là :
· CRISPR : des variétés de riz résistantes à la pyriculariose, du blé résistant à l'oïdium, du millet tolérant à la sécheresse
· Sélection génomique : réduction des cycles de sélection de 10-15 ans à 5-8 ans
· Phénotypage haut débit : analyse de milliers de parcelles en quelques heures, contre des semaines en méthodes manuelles
· Exploitation des ressources génétiques : identification de gènes de tolérance aux stress dans les banques de gènes
Les premiers produits arrivent sur le marché (tomate GABA au Japon, pomme de terre Innate aux États-Unis) et d'autres sont en phase avancée de développement. Le cadre réglementaire européen, actuellement en discussion, sera déterminant pour la capacité de l'Europe à rester dans la course.
Pour les jeunes entrepreneurs, le champ est vaste : services de phénotypage, développement d'algorithmes d'IA, conseil réglementaire, valorisation des ressources génétiques, formation. L'enjeu est de taille : contribuer à une agriculture capable de relever les défis du changement climatique, de la sécurité alimentaire et de la durabilité environnementale, en s'appuyant sur le meilleur de la science et de l'innovation.